Psychophysiologie : CM n°7 à 12
Psychopharmacologie
Introduction :
Niveau de complexité :
Les problèmes et considération sont différentes selon les niveaux des structures (molécules, synapses, neurones […] système cognitif, plus haut). Le tout apparaît comme supérieur à la somme des parties pour les organismes. La mise en relation des processus élémentaires qui sous-tendent les comportements est donc difficile du fait de la liaison qui n’est pas directe entre les différents niveaux.
Si le cerveau était assez simple pour qu’on puisse le comprendre, il serait sans doute trop simple pour comprendre quoi que ce soit. C’est un paradoxe épistémologique…
Le cerveau, le neurone et l’animal :
Il existe une certaine variété de cerveaux, différences individuelles n’induisant pourtant aucune pathologie particulière. Certains mécanismes de réparation dans le cerveau ne sont ni compris, ni imitables.
Nous avons entre 10 et 100 milliards de neurones. Dans un mm3 (voxel), on peut compter jusqu’à 600 millions de neurones au niveau du cortex. Si l’on multiplie la taille d’un neurone par 1000, on aurait un soma de la taille d’une tête d’épingle et des dendrites de l’épaisseur de quelques cheveux. Pour un neurone moteur, l’axone ferait alors 200m de long.
Tous les éléments constituant le cerveau humain se retrouvent chez d’autres animaux. La question est de savoir déterminer la présence des facultés (cognitives) supérieurs chez l’Homme malgré l’absence d’éléments nouveau (excepté une densité plus grande de neurones et dendrites).
Les facultés mentales comme la pensée, l’abstraction, les processus de conscience, peuvent être considérés comme spécifiques à l’Homme. Cependant, il est rare de pouvoir l’étudier directement et donc l’étude d’animaux apporte des biais nombreux.
Origine des psychotropes :
La synapse est le lieu d’action des psychotropes qui augmentent ou diminuent l’activité de celle-ci.
Les premiers psychotropes ont été découverts par « hasard ». Delay a développé les premiers neuroleptiques en 1952.
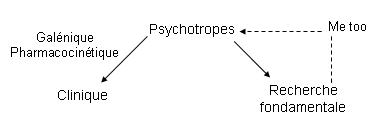
Galénique : présentation du médicament (cachet, pilule etc.).
Pharmacocinétique : comportement des médicaments dans l’organisme.
Me too :
- Amélioration des molécules déjà existantes.
- Variation autour d’une tête de file.
- Strip tease (modifications et simplification d’une molécule).
- Ressemblent à la molécule mère et gardent la même activité globale.
- Méthode de proche en proche.
- Moins d’effets secondaires
- Toute molécule nouvelle est une molécule inconnue.
- Médecins et malades apprécient l’existence de produits similaires qui ne le sont peut être pas tant que ça.
- Plagiat
Les outils thérapeutiques ont été donné à la psychiatrie avant de savoir quelles étaient leurs actions chez l’Homme et on ne sait toujours pas comment ils fonctionnent exactement.
Les années s’accumulent mais les choses n’évoluent pas mis à part les nouveaux neuroleptiques atypiques et nouveaux anti-dépresseurs.
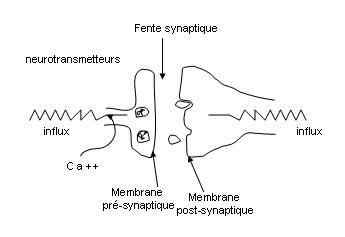
La synapse :
|
L’influx nerveux permet l’entrée de calcium. Ce calcium est nécessaire à la libération du neurotransmetteur. La fixation du neurotransmetteur sur le récepteur post-synaptique engendre un nouvel influx nerveux. |
Complications :
En réalité, un neurone a en moyenne 10.000 à 100.000 synapses ce qui en fait un système très complexe.
Les neurotransmetteurs « classiques » :
Ach – Acétylcholine Gly - Glycine
DA – Dopamine Glu - Glutamate
Na – Noradrénaline Asp - Asparate
5-HT – Sérotonine GABA
HA – Histamine Neuropeptides
Les neurotransmetteurs concernés dans la majorité des psychotropes sont la dopamine, la noradrénaline et la sérotonine. La dopamine n’a pas de fonction propre mais on la retrouve dans des phénomènes lis à la toxicomanie, la dépression, le Parkinson et la schizophrénie.
La barrière hémato-encéphalique (BHE) permet au cerveau d’être à la fois l’organe le plus fragile mais aussi le mieux protégé. En effet, bien que les neurotransmetteurs se trouvent partout dans le corps, il n’y a pas mélange entre les substances du corps et celles du cerveau (difficulté supplémentaire dans la mise au point de médicaments).
Exemple : les démences séniles de type Alzheimer (DSTA) et l’acétylcholine :
Données neurophysiologiques à propos de la maladie d’Alzheimer :
- C’est une affection dégénérative du cortex cérébral.
- Des protéines dites amyloïdes s’accumulent sous forme d’agrégats dans les tissus.
- Il y a diminution drastique de l’activité des neurones cholinergiques.
- Il y a perte sélective des neurones cholinergiques au niveau de l’hippocampe et du cortex frontal.
- L’évolution va vers une dépendance totale du sujet, un état grabataire.
- C’est un problème médical, social et économique.
- L’utilisation des inhibiteurs de l’acétylcholine (IACE) chez l’animal prolonge l’activité cholinergique en inhibant la destruction de l’acétylcholine.
La fin du vide thérapeutique se fait sentir avec l’apparition de Cognex (tacrine) en 1994 (4 prises par jours, toxicité hépatique), d’Aricept (donezepil) en 1998, Excelon (rivastigminie) en 1998 et Reminyl (galantamine) en 2000 (avec un effet nicotinique) mais ils ont une faible efficacité, fonctionnent pour des formes légères à modérées et ont de nombreux effets secondaires.
Il y a eu des avancées considérables de la recherche dans ce domaine. Le diagnostic est tardif et peu fiable. Le traitement médicamenteux n’est que symptomatique, palliatif. Il n’y a rien sur la mémoire mais seulement amélioration des fonctions cognitives, des troubles psycho-comportementaux.
Environ 10% des sujets traités ont un bénéfice dans les 6 premiers mois. La prise en charge est essentiellement médico-sociale. Il y a donc dichotomie entre la recherche fondamentale et les résultats pratiques.
Les neurotransmetteurs « non médiatiques » :
L’anandamide est un neurotransmetteur équivalent au principe actif du cannabis de la famille des endocannabinoïdes. Le mode de synthèse est différents des autres neurotransmetteurs puisqu’il est fabriqué à la demande (donc non stocké) à partir d’un précurseur, un lipide de la membrane cellulaire.
Acomplia ® (rimonabant) est un médicament en phase III d’étude clinique et est prévu pour 2006. C’est un antagoniste des récepteurs CB1 (cannabinoïde) qui serait un anti-tabagique, anti-obésité (sous conditions), avec amélioration du cholestérol et diminution des risques cardio-vasculaires.
Interaction entre les différents neurotransmetteurs (modèle de Calder) :
Il ne faut pas confondre cible primaire et secondaire : affecter un neurotransmetteur va forcément affecter les autres. On ne connaît pas exactement le résultat d’un traitement, ce qui pose des problèmes pour les traitements chroniques.
Co-localisation et co-transmission des neurotransmetteurs :
La loi de Dale veut qu’à un neurone soit associé un neurotransmetteur. Pourtant en observant des neurones, on a pu distinguer plusieurs neurotransmetteurs (2 à 9) pour un neurone : il peut donc y avoir co-localisation qui peut entraîner une co-sécrétion (libération simultanée de plusieurs neurotransmetteurs à l’arrivée du potentiel d’action).
Des expériences ont montré qu’en imposant une fréquence élevée de potentiels d’action, il y a libération des neuropeptides alors que pour une fréquence basse, il y a libération préférentielle du neurotransmetteur.
Les psychotropes actuels ne peuvent pas interagir avec les neuropeptides.
Neurotransmission locale :
La neurotransmission classique est sur le modèle du « point par point » : les neurones émetteurs ont des projections axonales vers les dendrites ou soma d’autres neurones. Cependant, il y a parfois neuromédiation chimique locale : des neurotransmetteurs libérés vont diffuser dans un rayon d’action dépendant de leur quantité. Il n’y a alors pas de fente synaptique et d’éléments post-synaptiques identifiés. La propagation se fait de proche en proche.
Les récepteurs :
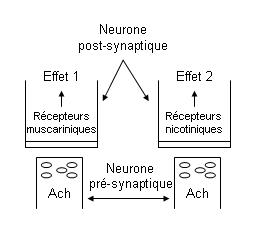
Avancées respectives de la biochimie et de la pharmacologie :
|
Pour obtenir spécifiquement l’effet 2 : - Physiologiquement : avec l’Ach. - Expérimentalement : Ach en injection intrasynaptique ou en utilisant la nicotine, agoniste spécifique des récepteurs du même nom. |
La biochimie a identifié de nombreux récepteurs différents pour lesquels on ne dispose pas (encore) de molécules spécifiques. Il serait possible de créer des molécules n’existant pas dans la nature, qui seraient spécifiques de ces récepteurs.
La grande inconnue est qu’on ne connaît pas la forme spatiale de toutes les molécules car cela demande beaucoup d’investissement et de travail.
Régionalisation, internalisation et down/up régulation :
Il existe une certaine proportion (faible) de récepteurs extrasynaptiques (régionalisation des récepteurs) ce qui permettrait de comprendre la communication extrasynaptique. Les cellules gliales jouent aussi un rôle important dans la modulation du signal et peuvent transmettre les neurotransmetteurs aux neurones.
L’apparition ou la disparition des récepteurs peut être très rapide (quelques minutes). Il peut y avoir formation très rapide de vésicules intracellulaires post-synaptiques contenant des récepteurs fonctionnels. Ce phénomène est parfaitement réversible.
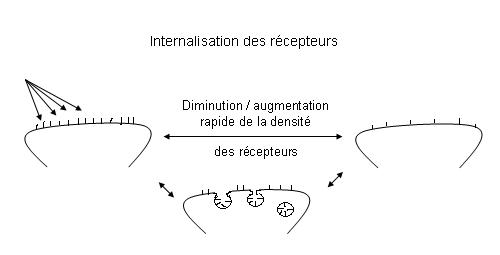
S’il y a moins de récepteurs, il y a diminution de la réponse fonctionnelle. C’est pour se « protéger » de l’arrivée massive d’une molécule que le nombre de récepteurs est réduit.
La « down-régulation » est la dégradation des récepteurs après stimulation prolongée. Il s’agit d’un phénomène plus lent (semaine / mois). L’organisme peut donner l’impression d’un manque apparaissant comme irréversible. On pense qu’il se passe un phénomène irréversible introduisant un déséquilibre à la suite d’exposition trop prolongée et massive à une substance.
Evolution plus ou moins spontanée de l’architecture neuronale :
Selon des condition d’évolution de rats (seuls, à plusieurs, à plusieurs avec des jeux) on s’aperçoit que plus l’environnement s’enrichit, plus l’arborisation dendritique est dense. La substance fine du cerveau apparaît donc comme modifiable par l’environnement. Si on reproduit l’expérience avec des rats adultes (ayant évolués jusque là dans un milieu intermédiaire) on obtient les mêmes résultats. Le cerveau adulte reste donc sensible à l’environnement. Le cerveau apparaît ainsi comme encore plus complexe par son aspect dynamique.
L’Homme apparaît comme l’espèce la plus épigénétique (interaction avec l’environnement), ce qui renforce l’aspect dynamique et individuel du cerveau humain.
La plasticité neuronale via la maladie de Parkinson :
La maladie de Parkinson concerne environ 1% de la population de plus de 60 ans et se traduit par une dégénérescence progressive des neurones dopaminergiques de la substance noire (tronc cérébral). On distingue trois symptômes majeurs : le tremblement de repos, la rigidité des membres et l’akinésie (impossibilité d’effectuer des mouvements voulus). L’évolution est relativement longue (20 ans environ) et la maladie peut s’associer avec divers troubles nerveux et psychiques. Les symptômes apparaissent quand le malade a moins de 20% de ses neurones de la substance noire. Avant, il y a des systèmes de compensation pour pallier la diminution du nombre de neurones : l’arborisation des neurones survivants se développe (bourgeonnement) pour prendre la place des neurones morts et ainsi les remplacer.
Thérapeutiques non pharmacologiques :
La sismothérapie (électroconvulsivothérapie, ECT) :
En 1938, Cerletti a constaté qu’un courant transcérébral ne tue pas et provoque une crise d’épilepsie généralisée typique. Les premiers essais sont effectués sur des schizophrènes sans anesthésie, ni curarisation. Les sujets ont présentés des améliorations mais les crises sont très spectaculaires. Cependant, le champ d’application sera abusivement répandu.
Delay va mettre au point la sismothérapie en introduisant l’anesthésie et le curare, ce qui fait que les mouvements sont indolores et à peines visibles. La patient se réveille dans un délai de 3 à 4 minutes, reste confus environ une demi-heure et est sur pied au bout d’une heure. Il n’y a plus de méthode apparaissant comme violente. Cette méthode sera largement désaffectée avec l’arrivée des neuroleptiques et des anti-dépresseurs mais il reste des indications indiscutables dans le cas de dépressions résistantes, accès maniaques résistants aux neuroleptiques etc.
Le mode d’action est inconnu (tout comme pour les défibrillateurs cardiaques). L’effet apparaît après un certain nombre de séances. Les effets secondaires se limitent principalement à une amnésie forte à priori nécessaire à une certaine restructuration. C’est une technique très peu iatrogène (causant des problèmes ; 1 décès pour 10.000 patients, dus à l’anesthésie). On prévoit 2/3 séances par semaine avec 6 à 12 séances pour un état mélancolique, 8 à 12 pour un état maniaque et 15 à 20 pour les délires schizophréniques. On ne persiste pas en cas de non-évolution. Le traitement est arrêté dès que l’état du patient est amélioré. Il n’y a pas de contre indication (sauf hypertension intracrânienne).
L’électroconvulsivothérapie permet l’amélioration rapide de certains patients par le cours à l’équivalent d’une crise convulsive provoquée par un courant électrique faible et très bref appliqué à la surface du crâne. L’ECT est indiquée (entre autre) dans les dépressions mélancoliques sévères réfractaires aux antidépresseurs. Elle est efficace dans plus de 90% des cas, est indolore, parfaitement bien tolérée et sans effets secondaires majeurs. Le délai d’action est court. En cas de rechute, cette méthode garde son efficacité. Il n’y a pas de lésions cérébrales objectivables par les techniques actuelles d’imagerie (pas de détérioration intellectuelle, ni d’induction de crises épileptiques).
Electrostimulation : une alternative à la dopathérapie :
La dopathérapie est une thérapie substitutive à un manque de dopamine dans le cerveau. C’est un traitement symptomatique qui est devenu le traitement de référence depuis les années 70. On a cherché à reprendre ce modèle de substitution pour d’autres maladies (Acétylcholine pour Alzheimer par exemple) mais ça ne fonctionne pas. Le traitement de la maladie de Parkinson par la dopathérapie semble être une exception mais l’efficacité est limitée dans le temps.
L’électrostimulation peut s’adresser aux parkinsoniens souffrant de complications motrices invalidantes. Il s’agit d’une stimulation cérébrale profonde chronique par l’implantation d’électrodes au niveau du noyau subthalamique. Elle se met en place par une opération réversible, ajustable et adaptable dans le temps, pratiquement dépourvue de complications (pas de destruction cérébrale définitive). Cependant, l’opération est très délicate. On constate aussi un effet antiépileptique obtenu par une stimulation aiguë ou chronique intermittente du nerf vague à la base du cou. Le mode d’action est inconnu et on a des indications pour la dépression.
Un point d’histoire : la psychochirurgie :
C’est l’ensemble des techniques chirurgicales ayant pour but de modifier le comportement : lobotomie qui consiste en la section d’un faisceau de substance blanche reliant le thalamus au lobe préfrontal. Elle a débuté en 1935 avec Moniz. On compte environ 100.000 interventions de ce genre entre 1935 et 1974 dont 50.000 aux Etats-Unis. C’est une technique simple et peu coûteuse.
C’est devenu un sujet tabou. Il s’agissait d’opération graves (au moins éthiquement) et irréversibles, sans le consentement du patient et partant du postulat qu’à une région correspondrait une fonction. Il n’y a pas de consensus sur les régions à opérer. Ces opérations pouvaient entraîner des apathies psychiques : certains patients deviennent moins agressifs par exemple.
Stimulations cérébrales profondes et troubles psychiques :
On a constaté des cas d’épisodes dépressifs aigus ou troubles comportementaux divers (rires, colères) au cours d’une stimulation centrale profonde chez une patiente (électrostimulation chez des parkinsoniens à priori mal placée).
Dans le cas d’un patient atteint de TOC sévères, résistants à tout traitement et suivi depuis Juin 2002, on a implanté deux électrodes dans le noyau caudé perturbé par les TOC. On observe pour une stimulation :
- aiguë : aucun effet.
- pendant 3 semaines : TOC toujours présents mais le patient n’est plus anxieux ni dépressif.
- pendant 3 mois : rémission profonde des troubles.
Il s’agit d’une technique en plein essor mais aux indications très limitées pour des raisons éthiques. Les interventions doivent s’inscrire dans un cadre de rechercher. Il y a dans cette technique non implication d’un lieu mais perturbation d’un réseau lié à une pathologie.
Thérapeutiques pharmacologiques :
Les agonistes :
Une molécule agoniste est toute substance capable de se lier avec un récepteur et par cette liaison d’entraîner une action biologique de même nature que le neurotransmetteur correspondant à ce récepteur. Le neurotransmetteur est un ligand endogène, naturel, physiologique alors que l’agoniste est un ligand exogène, synthétique, pharmacologique. Il y a aussi une différence de durée d’action : très peu de temps pour le neurotransmetteur et plus longtemps pour l’agoniste.
La supplémentation en L-Dopa :
La dopamine ne passe pas la barrière hémato-encéphalique. On utilise la L-Dopa qui est un précurseur de la dopamine et passe très bien cette barrière. La L-Dopa est transformée en dopamine grâce à une enzyme présente dans le cerveau. La dopamine a ainsi un effet ciblé sur le cerveau puisqu’elle ne peut pas non plus repasser la barrière hémato-encéphalique dans l’autre sens.
Le syndrome pseudo-parkinsonien rencontré chez des schizophrènes sous neuroleptique pourrait s’expliquer par le fait que les neuroleptiques font chuter le taux de dopamine sous le seuil « parkinsonien ». Inversement, un excès de L-Dopa chez un parkinsonien peut entraîner des hallucinations (trop de dopamine). Si une personne est potentiellement parkinsonienne infra-clinique (taux de neurones dopaminergiques encore supérieur à 20%) et se voit administrer une dose de neuroleptique on peut observer les effets de la maladie de Parkinson. Dans ce cas, on confirme le diagnostic de la maladie de Parkinson bien que la maladie ne soit pas encore apparente.
Héroïne – Méthadone et Subutex ® :
L’héroïne est la diacétylmorphine. Elle passe rapidement la barrière hémato-encéphalique et est transformée en morphine qui reste piégée dans le cerveau. Les effets sont plus précoces, plus intenses, plus brefs. Il y a pharmacodépendance, pas de consommation modérée et l’explication de cette dépendance est due à la pharmacinétique (rapidité d’action). En 1973, on identifie les récepteurs aux opiacés.
La méthadone est un opioïde sucré non injectable qui se prend quotidiennement par voie orale. L’alliance de la méthadone au sucre fait qu’elle est stockée dans le foie et sera libérée, avec le sucre, durant toute la journée de façon stable et sans pic : sans effet de manque. Il s’agit d’un médicament de substitution n’induisant qu’une toxicologie douce et permettant une possible réinsertion.
Le Subutex ® est l’alter ego de la méthadone. C’est un agoniste partiel de la morphine : les effets plafonds ne seront jamais maximum. Il vient occuper les récepteurs auparavant stimulés par l’héroïne. Il prévient la sensation de manque, est délivré sur ordonnance du médecin de ville. Sur 150.000 héroïnomanes, 70.000 sont sous Subutex ®.
On peut considérer que le toxicomane est un malade chronique accessible au traitement. On a énormément de mal à obtenir un sevrage complet (même si les doses ont été extrêmement réduites). C’est quand les récepteurs ont été bien « nettoyés » (séjour à l’hôpital, en prison) que le risque d’overdose est avéré.
Les antagonistes : exemple de l’Anexate ® :
Alors qu’une substance agoniste stimule le récepteur, une substance antagoniste le bloque. Elle occupe son site sans engendre de réaction. Il n’y a pas de substances antagonistes dans le corps humain à l’état naturel.
L’anexate ® intervient dans les cas de TSMM (tentatives de suicide médicamenteuses multiples). Elle permet d’éviter l’intubation et la ventilation assistée. La substance déloge la benzodiazépine des récepteurs et occupe la place : le sujet se réveille donc. Vu l’efficacité du produit, on préfère l’injecter à dose non maximale pour provoquer un réveil progressif et non instantané. Cette substance s’utilise à l’hôpital et non sur place. Elle facilite aussi le réveil après une anesthésie. De même, la maloxone est un antagoniste des opiacés.
Le lithium :
C’est un élément très simple (ion Li+, troisième élément après l’hydrogène et l’hélium). Il n’agit que sur les PMD (psychoses maniaco-dépressives). Il n’y a pas d’accoutumance mais le traitement est à vie et en cas de traitement discontinu il peut y avoir apparition d’une résistance au traitement. Le lithium n’a aucun effet sur un sujet sain, il y a peu d’effets secondaires et on ne peut pas prévoir si un sujet répondra au traitement ou non. Il n’y a pas de modèle animal pour la recherche (pas de PMD apparente chez les animaux étudiés). Le mode d’action est intracellulaire par les protéines G. Le lithium est un élément non probant : malgré son efficacité et sa spécificité, il est présenté avec les autres traitements et ne permet pas d’expliquer la PMD. Il y a une nette différence entre la fréquence de prescription attendue et celle observée (sous utilisé).
Le Prozac ® :
C’est un inhibiteur spécifique de la recapture de la sérotonine (SSRI). Il n’y qu’une prise par jour, une seule dose et une bonne tolérance ainsi que des effets secondaires réduits. C’est un « me too » présenté comme « clean ». Mais c’est devenu un miracle commercial, co-proscrit dans des maladies ayant une répercussion sur le moral par exemple. C’est devenu un produit de consommation adapté au type de société occidentale.
Il y a eu extension des indications : TOC (1993), dépression, pathologies alimentaires, syndrome prémenstruel, prévention des attaques de panique, anxiété généralisée, phobie sociale etc.
Les principaux atouts du Prozac ® sont sa précision d’action (SSRI), la pauvreté d’effets secondaires et son champ d’action large. Mais les effets sont surestimés et, comme tous les antidépresseurs, il peut y avoir virage maniaque. Le peu d’effet secondaire fait qu’on continu le traitement plus longtemps.
Evolution du concept de toxicomanie :
On a :
- des drogues avec toxicomanie : tabac, alcool etc.
- des toxicomanies sans drogue : relation avec une activité, travail, sport, télévision, jeux, voiture (conduite à risque, sexe, recherche de sensations, Internet, etc.
- des drogues sans toxicomanies : méthadone, cocaïne, Prozac (mythe de la drogue parfaite, médicament psycho-actifs sans autodestruction).
Conclusion :
La psychiatrie est la seule branche de la médecine sans localisation anatomo-pathologique. Par référence avec la neurobiologie et en opposition fondamentale avec cette dernière, la psychiatrie n’a pas de base structurale identifiable.
Les hypothèses concernant une perturbation cérébrale ne restent que des hypothèses.
L’action des drogues sur un système de neurotransmetteurs ne ressemble en rien à l’activité biologique spontanée de ce système.
La complexité de la biochimie du cerveau indique à l’évidence qu’il est difficile d’imaginer à partir de base rationnelle des agents psychopharmacologiques.